
Signature Q100作为一款自动化、高灵敏、高通量的蛋白组定量分析系统,利用微流控技术自动构建纳升级反应体系,可实现在1ul体液样本中检测多达96个蛋白标志物(在14ul体液样本中实现1160重蛋白标志物检测),让您在单一系统上轻松实现从中到高通量的实验需求。
目前,olink针对不同研究需求,可提供心血管、肿瘤、肿瘤免疫、免疫反应、炎症、神经、代谢、器官损伤等多个方向的96~3072 panel系列检测,被广泛地运用到科学问题的探索研究中去,包括疾病预测&预后生物标志物的筛选、患者分层诊疗、疾病发生的机制机理,药理药靶的研究等等。
应用领域:
1、人类健康管理一监测生活方式与疾病的关联;2、疾病分型;3、疾病早筛与预后诊断;4、寻找新的药物靶点;5、药物安全与疗效检测;6、更好的理解生物学机制;7、药物研发;8、基础研究;9、医学转化;
应用案例分享
1)、2023年10月三篇Nature重磅:揭开了大规模血浆蛋白质组在精准医学领域广泛应用

UKB-PPP联盟的Benjamin B. Sun博士等人的最新旗舰论文,文中报道发现了14,000多个蛋白质表达水平相关的遗传关联,且其中81%为最新发现,清楚地表明了高通量蛋白质测量对于识别重要生物途径及其对健康影响的重要性。具有里程碑意义。

阿斯利康基因组中心及药物发现团队:Ryan S Dhindsa博士等人联合发表,研究了罕见蛋白质编码变异与蛋白质表达之间的遗传关联,揭示了罕见变异在血浆蛋白质水平改变和生物结果中的重要作用,进一步凸显了大规模蛋白质组学研究对于实现此类发现的关键需求,并加速药物研发。
G. H. Eldjarn博士等人发表文章,将冰岛大规模人群队列研究数据结果做了两种技术对比,包括Olink蛋白组学平台和另一种基于适配体的技术。基于Olink蛋白组学平台数据结果显示,其与顺式pQTL相关性具有显著更高比例72%(与基于适配体技术的43%相比),中位数变异系数(median CV ratio)更低,表明Olink平台具有更高特异性,和平均值更精确。
2)、香港科技大学叶玉如院士团队发现21种新核心蛋白用于AD疾病的早筛及分期

叶玉如院士团队一直致力于阿尔茨海默症诊断和治疗方法的研究。该团队通过Olink高通量超灵敏多因子检测系统,对 AD 进行了大规模血浆蛋白质组检测分析,发现了数百种与 AD 相关的血液蛋白质生物标志物,其水平变化与 AD 进展和分期有关。经机器学习的数学模型后,开发出了一种包含CASP3、CD33、CD84、EIF4B等21种核心血液蛋白标志物的评分系统,准确鉴定AD并确定AD患者疾病严重程度。通过血液生物标志物无创检测,可将阿尔茨海默症的早期诊断提前5-10年,且方法可用于评估患者病情阶段。

21 种血液蛋白变化与 AD、MCI(轻度认知障碍) 和 AD 相关的表型关联:
通过线性回归分析确定了每种蛋白质水平与AD、MCI及其相关内表型之间的关系,并调整了年龄、性别、心血管疾病状况(即心脏病、高血压、糖尿病和高脂血症)和体重指数影响,21种蛋白质在AD患者血浆中都出现了明显改变(上图):9种蛋白上调,12种蛋白下调。与正常认知(CN)相比,MCI 患者血浆中 18 种血液蛋白水平发生了变化,这表明这些蛋白在早期 AD 中调节失调。此外,有几种血液蛋白与AD相关表型有关,即血液中ATN生物标志物失调、MoCA评分显示的认知能力下降及灰质&海马体积减少。

AD风险评分系统可准确分类AD与MCI:
根据 21 种蛋白的血浆水平为个体生成 AD 风险评分(下图 A),在香港华裔队列_1中,AD风险评分准确地将AD患者(AUC = 0.9667)和MCI患者(AUC = 0.8718)与CN个体区分开来(下图B-D)。在 357 名参与者的子队列中,比较了血浆 ATN 生物标志物与 21 种蛋白标志物检测在 AD 和 MCI 分类中的表现。结果显示,血浆 NfL(AUC = 0.9177)、血浆 p-Tau181(AUC = 0.9656)和 21 种蛋白标志物检测(AUC = 0.9667)区分 AD 患者和 CN 患者的准确率均大于 90%,而血浆 Aβ42/40 比值的准确率相对较低(AUC = 0.6654)(下图 C)。而且,在区分 MCI 患者和 CN 患者时,21 蛋白质标志物检测的准确率大于 85%(AUC = 0.8718),而血浆 Aβ42/40 比值(AUC = 0.5305)、血浆 NfL(AUC = 0.7790)和血浆 p-Tau181 (AUC = 0.6510)的准确率相对较低(下图 D)。
3)、CORAL 联盟发表Nature Communications:通过Olink蛋白质组学,鉴别路易体痴呆症与阿尔兹海默症

该联盟利用Olink蛋白组学技术,对血液和脑脊髓液(CSF)样品进行一系列研究,以深入研究神经疾病的致病机制、生物标志物,干预后有效标志物及预测指标等。
该研究使用Olink 蛋白组学技术,检测了认知未受损对照组(n=190)、DLB患者组(n=190)与AD患者组(n=235)脑脊液(CSF)中的蛋白质表达水平,找出差异表达蛋白并进行分组建模。同时采用Olink定制化检测panel用于临床转化,在三个独立验证队列中进行了验证,确定了DLB患者特异性的蛋白质变化,并将发现转化成了可准确识别BLD患者的定制化panel,为DLB患者的诊断和临床治疗提供了希望。
4)、中山大学肿瘤医院陈丽昆教授团队Oncoimmunology杂志发表,利用Olink蛋白组学技术预测肺癌脑转移患者颅内免疫治疗响应

研究入组了28位接受camrelizumab(卡瑞利珠单抗)联合化疗的初治NSCLC脑转移患者,在基线和首次治疗评估时前瞻性地收集了配对血浆和脑脊液样本,使用Olink Target Panel对所有样本进行了92种免疫肿瘤细胞因子分析:
1、脑脊液中的大多数免疫细胞因子,在基线时表达显著低于其在血浆中的表达(下图),而包括CD83、PTN、TNFRSF21、TWEAK、ICOSLG、DCN、IL-8和MCP-1在内的一个亚群在脑脊液中表达相对较高。
2、与非响应者相比,颅内肿瘤响应患者脑脊液LAMP3基线水平显著较高,而CXCL10、IL-12、CXCL11、IL-18、TIE2、HGF、PDCD1水平显著较低。在多变量分析中,研究人员发现脑脊液中的LAMP3与颅内响应显著相关。
5)、哈佛医学院Nature 重磅:MGH 团队采用类器官模型与血浆蛋白质组学发现克服免疫逃逸新靶点TBK1
 
免疫检验点阻断剂(Immune checkpoint blockade, ICB)是增强免疫系统对各种癌症反应的重要药物,但一些患者的癌细胞会在治疗过程中产生耐药性。
哈佛医学院麻省总医院 癌症研究中心的研究员Russell W. Jenkins 博士等人,在混合遗传筛选中识别了TANK 结合激酶 1 (TBK1) 基因作为潜在的免疫逃逸基因。在多个实验模型系统中使用一套遗传和药理学工具,他们确认了 TBK1 作为免疫逃逸基因的作用。靶向 TBK1 通过降低效应细胞因子 (TNFα/IFNγ) 的细胞毒性阈值来增强对 PD-1 阻断的反应。 TBK1 抑制联合 PD-1 阻断也被证明了在患者来源的肿瘤模型中的有效性,且在患者来源的器官型肿瘤球体 (PDOTS) 和患者来源的类器官 (PDO) 中具有一致的发现。缺乏 TBK1 的肿瘤细胞以 JAK/STAT 依赖的方式响应 TNFα/IFNγ ,以启动RIPK 和 caspase 依赖的细胞死亡程序。结果表明,靶向 TBK1 是克服癌症免疫疗法耐药性的一种新颖而有效的策略。
6)美国西北大学范伯格医学院Cell (IF = 66.85 ):Olink助力多组学研究发现大脑老化机制相关脑脊液蛋白标志物
 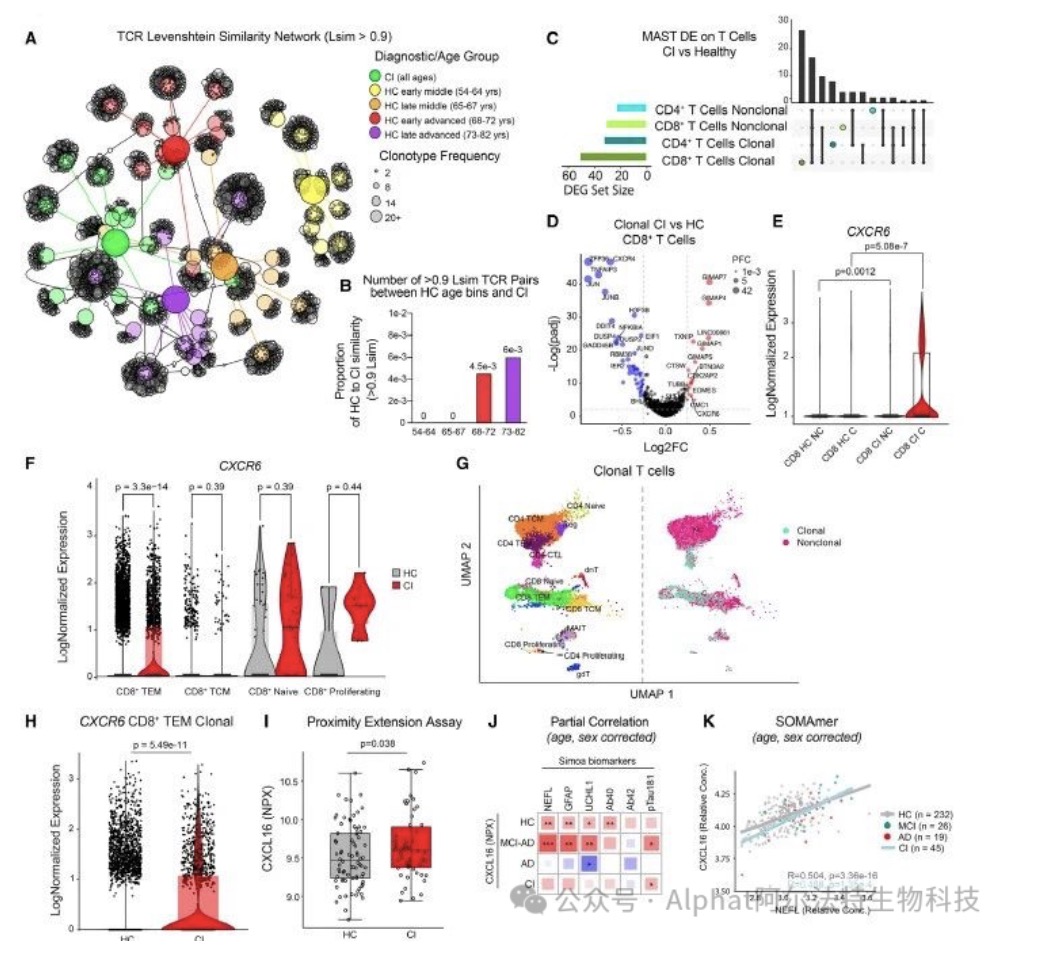
美国西北大学范伯格医学院的研究人员,开展多组学对45名认知正常受试者和14名认知障碍受试者的CSF 进行了系统研究,发现:
1、在认知正常者的CSF 中,单核细胞随年龄增长上调脂质加工基因;
2、在认知障碍者的CSF 中,单核细胞脂质转运基因失调;在认知障碍者的CSF 中,单核细胞通过CXCL16-CXCR6通路向克隆的CD8+ T细胞发出信号;CXCL16 在认知障碍者的CSF 中增加,并与神经变性有关。
7)、英国伦敦大学肺癌研究中心发表Nat Med (IF 82)研究:Olink Explore 3072 助力肺癌专项大队列研究发现恶病质新机制
 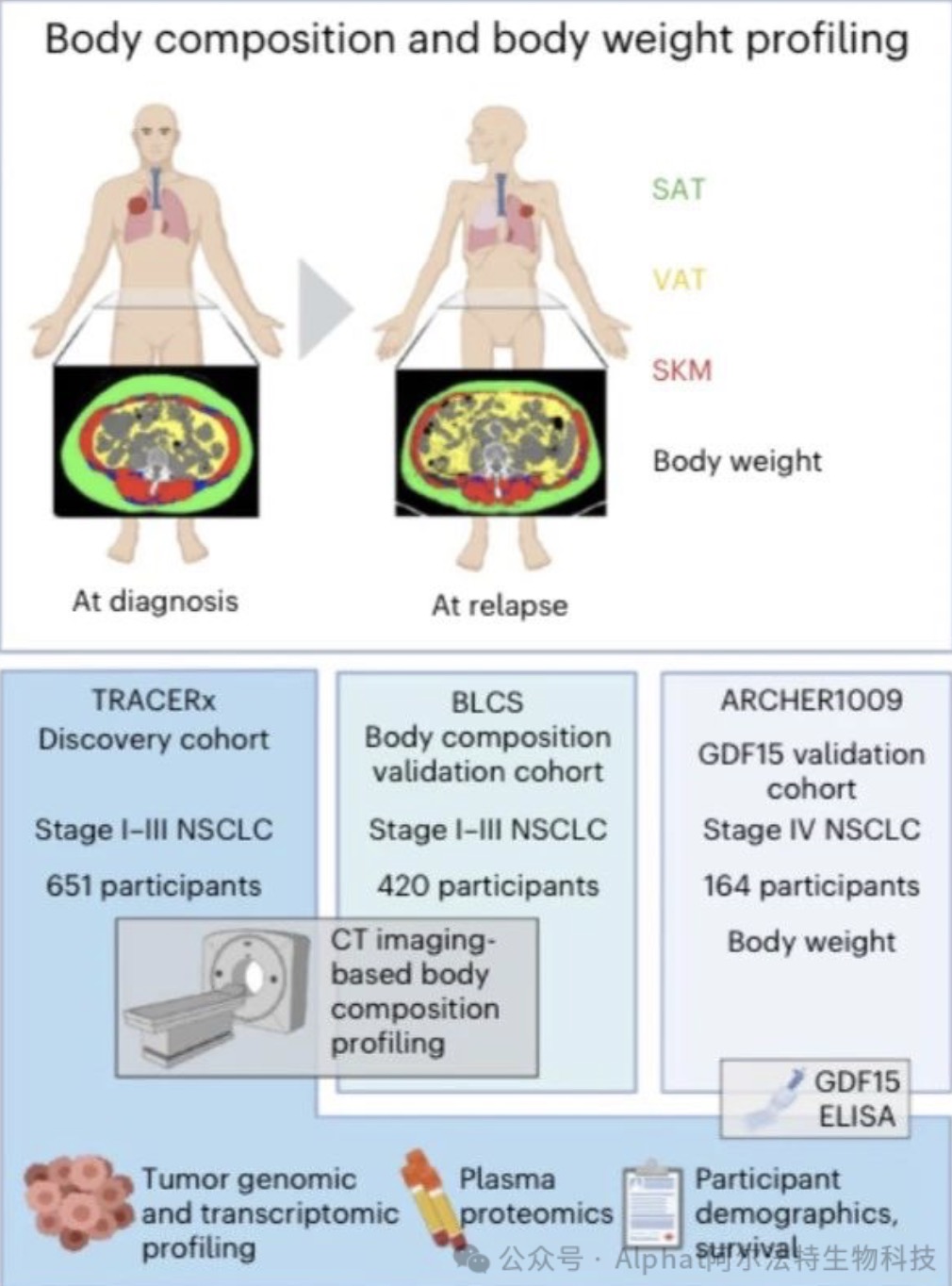
 英国伦敦大学肺癌研究中心TRACERx科研人员从基因组学、转录组学和蛋白组学三个层面对身体成分和肺癌相关肿瘤恶病质发病相关性进行了探索,Olink Explore 3072试剂盒用于血浆蛋白组学检测,发现: 英国伦敦大学肺癌研究中心TRACERx科研人员从基因组学、转录组学和蛋白组学三个层面对身体成分和肺癌相关肿瘤恶病质发病相关性进行了探索,Olink Explore 3072试剂盒用于血浆蛋白组学检测,发现:
1、患者在确诊时较低的肌肉和脂肪组织含量与较短的肺癌带病生存时间和总体生存时间相关。
2、患者身体成分以及体重的纵向变化与治疗效果相关,并可以被用于肺癌肿瘤恶病质的表型鉴定。
3、GDF15被确定为肿瘤恶病质的最明显血浆蛋白标志物,有潜力成为临床干预和治疗肺癌肿瘤恶病质的新靶点。在高通量蛋白组学检测中,对处于确诊初期的141名以及复发期的115患者进行血浆蛋白组学分析。72种蛋白质在有肺癌肿瘤恶病质的肺癌患者的血浆里有明显升高。9种蛋白质在非肺癌肿瘤恶病质的肺癌患者的血浆里有明显升高。
8)、上海交通大学瑞金医院Cell (IF = 66.85 ):Olink蛋白组学揭示奥密克戎患者接种疫苗后系统免疫图谱
 
上海交通大学瑞金医院陈赛娟院士、李庆云教授等,以2022年春季在上海流行的Omicron变异株为研究对象,招募了122名受感染成人和50名未感染对照者,其分别接种了不同次数的COVID-19灭活疫苗。研究团队采用质谱流式、转录组及Olink血浆免疫蛋白质组,对外周血样本进行整合分析,揭示了增强针疫苗的接种诱导了单核细胞免疫反应,启动了单核细胞的激活和成熟,而不是分化为髓源性抑制细胞,首次揭示了加强针疫苗接种为Omicron感染者提供保护性免疫的系统免疫学分子机制。研究团队采用Olink Target 96 Inflammation 和Immune Response 两个Panel,评估了队列血浆样本中的180种独特的炎症和免疫反应相关蛋白。
【微信公众号:Alphat阿尔法特生物科技】
相关产品推荐:
1、Octet R2/ Octet@ R4 / Octet R8 生物分子相互作用分析系统
2、自动化细胞扩增系统
3、高通量活细胞长时间成像分析系统
4、Oxford Nanopore 第三代单分子纳米孔测序仪
5、应用案例分享 --- Oxford Nanopore 第三代单分子纳米孔测序仪
6、Ai 智能化共聚焦高内涵成像分析系统
7、超高分辨快速3D多重扫描共聚焦显微镜
8、360度3D全息无标记活细胞亚显微成像系统
9、细胞能量代谢分析仪 - 肿瘤细胞无氧呼吸能量代谢监测
10、MA900 多功能全自动流式细胞分选仪
11、SEM/TEM电镜-生物拉曼光谱成像联用系统
12、跨膜态大尺寸高清全景共聚焦组织流式定量定位分析系统
13、多光谱全景扫描组织流式定量定位分析系统
14、小动物多模态超高分辨光声成像系统(选配内窥镜)
|